La radioactivité
Les différents rayons
La radioactivité est issue de la désintégration du noyau de certains atomes lourds, instables, à ce moment, les atomes émettent une particule. Il y a trois formes d'émissions différentes :
- Les rayons alpha (composés de 2 protons et 2 neutrons) sont des éjections de particules facilement arrêté par une feuille ou encore par une couche d'air. Ils sont causes de brûlures superficielles sur la peau.
- Les rayons bêta qui consistent aussi en une éjection de particule, peuvent traverser une feuille mais pas un papier aluminium. Ils pénètrent plus loin dans l’organisme que les rayons alpha, jusque dans les couches superficielles de la peau.
- Les rayons gamma eux, sont des ondes seulement arrêtées par plusieurs dizaines de centimètres du plomb et qui pénètrent dans l'organisme en provoquant des dégâts conséquents sur leur passage.
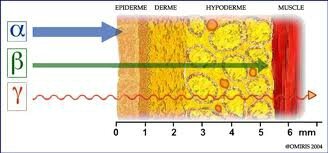
Zone d’action des rayonnements sur le corps
Dans ce schéma, nous voyons bien que les rayons alpha αatteignent seulement l’épiderme, c’est pourquoi ils causent des brûlures superficielles.
La flèche verte, représentant les rayons bêta β, traversent les couches superficielles de la peau (épiderme, derme, hypoderme) et causent des brûlures plus importantes.
Nous voyons bien que la flèche rouge (rayon gamma γ) passe au travers du muscle. Elle cause donc des dégâts plus conséquents.
Les éléments qui composent la radioactivité
La radioactivité se trouve à l'état naturel principalement dans les sous-sols où il y a du granite donc de l'uranium et parfois du radium. L'uranium est un métal lourd (comme le plomb ou le fer) qui a la particularité de dégager des rayons tellement pénétrants qu'ils pourraient traverser un matelas, de plus, dans n'importe quel milieu, il continue à rayonner de même manière. D'ailleurs, plus il y a de l'uranium dans un milieu, plus ce milieu est radioactif. Il existe plusieurs types d’uraniums (famille, isotopes), ils ont tous le même nombre d’électrons et de protons (92) mais des nombres différents de neutrons. A partir de la 6ème génération de désintégration, l'uranium 235 devient un gaz, le radon. Le radon, s'il est absorbé, devient solide dans l'organisme et se dégrade progressivement. C'est ce qu'on appelle la contamination. Ce n'est qu'à la 14ème génération que l'uranium deviendra stable et se transformera en plomb 206.
Le radium (d'un aspect totalement blanc mais qui noircit lors de son exposition à l'air libre) est un métal encore plus radioactif que l'uranium. Après sa découverte, il a été utilisé dans plusieurs produits tels que des crèmes rajeunissantes les cigarettes, les sodas atomiques, les poudres de riz, les dentifrices, les sels de bain, le talc pour bébé avant d'être interdit en 1937. Heureusement, le radium n'était pas toxique dans ces produits car il était si cher qu'il était incorporé en quantité infime.
Le polonium est un autre élément chimique hautement radioactif : l’absorption de 1 à 10 microgrammes est suffisante pour provoquer la mort. De plus, on estime qu'1% des cancers du poumon aux États-Unis est causé par cet élément. Le polonium est aussi utilisé comme source primaire au démarrage des réacteurs nucléaires ou dans le domaine spatial comme source d'énergie pour les satellites.
Présence
On trouve beaucoup d’éléments radioactifs dans l’espace : ils sont à l'origine de la formation des étoiles et des planètes. Il y en a aussi dans le sous-sol ce qui réchauffe la croûte terrestre. Ils sont aussi présents dans les végétaux et chez les animaux c’est pourquoi on peut trouver de la radioactivité dans les aliments.
Exposition
Les rayonnements radioactifs provenant de l’espace (étoiles, planètes) constituent 60% de nos expositions a la radioactivité. Nous sommes aussi exposés a des rayonnements artificiels (radiographie, déchets nucléaires) mais il est de l’échelle de 1%. D'autre part les maisons construites avec des pierres anciennes contiennent souvent de l'uranium donc de la radioactivité. Au delà d'une exposition de 1000 becquerel, le risque de cancer des poumons augmente.
Les effets de la radioactivité sont plus importants lorsque le noyau met le plus longtemps à se dégrader. Pour mesurer leur durée de vie (souvent très longue) on utilise la notion de « demi-vie ». Elle correspond à la durée pendant laquelle la moitié des noyaux radioactifs se désintègrent. Celle du radium par exemple est de 1602 ans.
Périodes radioactives de quelques radioéléments naturels
|
244Pu |
80×106 a |
||
|
Uranium 240 |
240U |
14,1 h |
|
|
Neptunium 240 |
240Np |
62 min |
|
|
240Pu |
6 560 a |
||
|
Uranium 236 |
236U |
23,42×106 a |
|
|
232Th |
14,05×109 a |
||
|
Radium 228 |
228Ra |
5,75 a |
|
|
Actinium 228 |
228Ac |
6,15 h |
|
|
Thorium 228 |
228Th |
1,19 a |
|
|
Radium 224 |
224Ra |
3,63 j |
|
|
220Rn |
55,6 s |
||
|
Polonium 216 |
216Po |
0,145 s |

/https%3A%2F%2Fstorage.canalblog.com%2F27%2F67%2F1320446%2F101022351_o.jpeg)
/https%3A%2F%2Fassets.over-blog.com%2Ft%2Fcedistic%2Fcamera.png)